铀矿科普—1铀元素
来源: 发布时间:2018年11月13日 17:08 作者:系统管理员

铀矿科普
铀元素
一、铀元素的发现
1789年,德国杰出的化学家、矿物学家M.H.克拉普洛斯(Martin Heinrich Klaproth,1743~1817),在一个极为普通的实验室里分析研究George Wagsfort矿山(德国)的沥青铀矿时,惊奇地发现了一种“新元素”。该“新元素”最初被命名为“Uranit”,是为了纪念F.W.赫歇尔(Friedrich Wilhelm Herschel,1738~1822)1781年发现的行星Uranus(天王星)。1790年最终将这个新发现的元素定名为“Uranium”,即铀,元素符号用英文字母U表示(Uranium的第一个字母)。它的发现在世界科技史上具有划时代的意义。
当时克拉普洛斯发现的铀只是铀的氧化物(二氧化铀)。52年后,法国化学家E.M.佩利戈特(E.M.Peligot)于1841年制得了金属铀,成为世界上制得金属铀的第一人。
铀元素发现后,一些物理学家开始注意研究铀的荧光现象,其中包括以研究铀盐而著名的法国物理学家亨利·贝克勒尔(Henri Becquerel,1852~1908)。1896年3月,亨利·贝克勒尔在实验中把未感光的底片用较厚的黑纸包好,再在黑纸包上涂上铀盐,然后置于阳光下照射,几小时后冲洗底片时,发现底片感光了,而且,底片上清楚地显示出铀盐覆盖的痕迹。后来,多次实验中他在包有底片的黑纸和铀盐之间放置各种物体试样,再经阳光照射,然后冲洗底片,他发现底片上同样留下了各种物体的影像。又经过多次实验,尤其是发现铀盐虽未经日光照射,包着黑纸的底片仍然曝光,他通过各种铀盐的反复实验和观测,发现一种由铀自然放射的、肉眼看不见、具有穿透性的射线,这种射线能使照相底片感光,还能使空气成为电的导体。因此,他断定“铀是一种能放出射线的元素”。这就是人类认识史上具有划时代意义的伟大发现—天然放射性的发现,它的发现和研究在科学界引发了一场真正的革命,开创了原子能研究的应用领域,使人类进一步迈向现代文明。随后居里夫妇也发现了另外两个能放射相似射线的元素——钋(Po)和镭(Ra),并确定了这些射线的特点,而将这种现象称作“放射性”。由于铀元素天然放射性的发现,亨利·贝克勒尔和居里夫妇于1903年共同荣获了诺贝尔物理奖。
|
|
|
贝克勒尔 | 皮埃尔·居里 | 居里夫人 |
二、铀的物理、化学性质
(一)铀的物理性质
铀在元素周期表中的位置 在周期表中,铀位于第七周期第ⅢB族,是锕系元素之一,与第六周期第ⅢB族镧系元素相对应。作为锕系元素,其电子层结构具有明显的特点,即具有O、P和Q层3个未饱和的电子壳层。
原子性质 铀的原子序数为92,以12C为基准得出铀的原子量为238.0289,是自然界至今发现的最重的元素,是重要的天然放射性元素。铀原子呈椭圆形,短轴半径为1.4Å,长轴半径为1.65Å,原子体积为12.59cm3/mol;密度大,常温下为19.05g/cm3,与黄金的密度(19.32g/cm3)相差不多;它的硬度稍低于铜的硬度,其布氏硬度为240~260kg/mm2;熔点1132.3℃,沸点3818℃,热导率(25℃)0.060卡/厘米·秒·度,电导率3.8×106S/m,比热6.594卡/摩尔·度,抗拉强度450MPa,屈服强度207MPa,弹性模数172GPa,在接近绝对零度时具有超导性和延展性(图1-1)。
原子结构 铀原子的中心为原子核,围绕带正电荷的原子核有数目与质子数相等的、带负电荷的电子不断运动,这些电子的运动均沿着一定的轨道,几个轨道组合在一起形成一个电子壳层。围绕铀原子核的周围运转的92个电子呈层状分布,即,铀原子有4个完全饱和的电子壳层K(2)、L(8)、M(18)、N(32)和3个未完全饱和的电子壳层O(21)、P(9)、Q(2),价电子层结构为5f36d17s2。
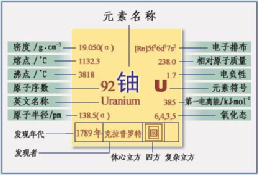
图1-1 铀元素性质
铀同位素 铀原子核由质子和中子构成。其中有92个质子,但所含的中子数是可变的,因而构成铀的各种同位素(具有相同质子数,不同中子数的同一元素的不同核素互为同位素)。迄今已发现质量数在226和242之间15个铀同位素,在自然界中存在的只有238U、235U和234U,它们的同位素相对丰度分别为99.275%、0.720%、0.005%,半衰期分别为45亿年、7.3亿年和26万年。其余12种同位素都是在核反应过程中由人工制取,同位素相对丰度仅为0.00n%~0.000n%,半衰期多数都很短。上述铀同位素都具有放射性,其中只有235U和238U是重要的核燃料。
单质铀 纯金属铀是人工制取的,呈银白色,微带淡蓝色调。铀具有金属光泽,粉末状金属铀呈灰黑色(条痕)。金属铀不是良导体。铀的顺磁性很弱,其随强度升高而增加。磁比率χm=414×10-6cm·g·s。
铀同素异形体 铀有α、β、γ 3种同素异形体。实验测定结果表明,α变体在667.7◦C时转变为β变体;当温度升高到774.8◦C时,它又转变为γ变体。当实验条件变化,压力为29.8千巴时,α、β、γ变体处于平衡的三相点(798℃即为1071K);当压力大于29.8千巴时,γ变体直接转变成α变体。
(二)铀的化学性质
铀的化学性质活泼,几乎能与所有的非金属作用(惰性气体除外),也可与多种金属形成金属互化物,也能与许多酸、碱、盐起反应。空气中易氧化,生成一层发暗的氧化膜,高度粉碎的铀在空气中极易自燃,块状铀在空气中易氧化失去金属光泽,在空气中加热即燃烧,250℃下与硫反应,400℃下与氮反应生成氮化物,1250℃下与碳反应生成碳化物,250~300℃下与氢反应生成UH3,UH3在真空350~400℃下分解,放出氢气。具有变价的特性,有+3、+4、+5、+6几种价态。
在自然界中,铀的稳定氧化态只有+4、+6价两种,+4价铀在还原条件下稳定,+6价铀在氧化条件下稳定。U4+呈弱碱性,当pH=2时发生水解,在溶液中呈绿色;U6+具有两性特征,但酸性较强,碱性较弱。
铀属亲石元素,与氧具有很强的亲和力。自然界中,铀总是以各种氧化物和含氧化合物的形式出现。铀的主要化合物包括铀的氧化物、铀的卤化物、铀盐等。主要的铀氧化物有二氧化铀(UO2)、八氧化三铀(U3O8)、三氧化铀(UO3)。铀卤化物主要有UF3、UF4、UF5、UF6、UCl3、UCl4、UCl5、UCl6。铀与各种酸作用可生成相应的盐类,如硝酸铀酰、氟化铀酰、硫酸铀酰等。
三、铀的放射性
放射性是指元素从不稳定的原子核自发地放出射线(如α射线、β射线、γ射线等)衰变形成稳定的元素而停止放射(衰变产物)的一种现象。这种不稳定的原子核自发地放出某种射线而转变成另一种原子核的变化过程,称为放射性衰变或核衰变。放射性核在衰变过程中遵守能量、质量及电荷守恒定律。原子序数大于82的元素因其原子核的不稳定性都具有放射性,铀(原子序数为92)是最容易发生放射性衰变的元素之一。
放射性核素(指具有放射性的、由一定数目质子和一定数目中子构成的原子)的衰变方式主要有α衰变、β衰变、电子俘获和同质异能跃迁。
α衰变:不稳定原子核自发的放出α粒子而转变成另一种原子核,这种衰变称为α衰变。
α粒子由两个中子和两个质子组成,它的质量数为4,带两个正电荷。α粒子是高速运动的氦原子核(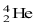 )。原子核经α衰变后产生的新原子核,其质量数减少4,原子序数减少2。
)。原子核经α衰变后产生的新原子核,其质量数减少4,原子序数减少2。
β衰变:不稳定原子核自发的放出β粒子和中微子而转变成另一种原子核,这种衰变称为β衰变。
β粒子是带有一定能量的电子。原子核经β衰变后产生的元素,其原子序数增加1,质量数不变。
β衰变有两种:即β+衰变和β-衰变。β+衰变是当原子核中质子过剩时,质子转化为中子而放出β+粒子和中微子;β-衰变是当原子核中的中子过剩时,中子转化为质子而放出β-和中微子。天然放射性核素的β衰变主要是β-衰变。
α、β衰变时常伴随放出γ光子。γ光子不带电,质量为零,波长很短,通常小于10pm(10-12m),其能量可达100keV~10MeV。放出γ光子的核变化称为γ衰变。γ衰变过程中,原子核放出的电磁波,即γ射线(γ光子)。
电子俘获:当原子核中质子过剩时,原子核中的质子从核外捕获一个轨道电子而变成一个中子,这种衰变称为电子俘获。
同质异能跃迁:衰变前、后核素的原子序数(Z)和质量数(A)都相同,只是能量不同(因衰变后原子核的能量由于放出γ光子而减少)的衰变称为同质异能跃迁。
放射性核素衰变时会放出射线,这些射线不是单一的,当射线通过电、磁场时就可以发现是一种分别为带正电荷的α射线和带负电的β射线以及不带电的γ射线(图1-2),其穿透能力为:α射线较弱,β射线较强,γ射线很强(图1-3),这些射线通过物质时,与物质发生作用,产生某些效应和现象。
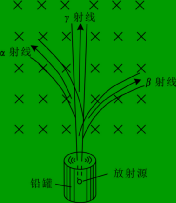
图1-2 α、β、γ射线
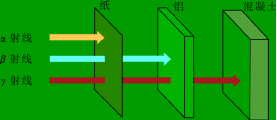
图1-3 α、β、γ射线的穿透能力
自然界存在3个天然放射性系列,即铀(U)系、钍(Th)系和锕铀(AcU)系。这3个天然放射性系列中,分别以238U、232Th和235U作为3个放射性系列的起始元素,它们的半衰期都很长,在1到100亿年之间。起始元素经过衰变,形成一个新元素称为衰变子体,但这个元素仍不稳定,将继续衰变下去,直至形成一种稳定的元素为止。每个系列中各有一个气态同位素,通常称为射气,原子序数为86,而206Pb、207Pb、208Pb则分别是3个放射性系列的最终稳定元素。起始元素称为“母体”,其他衰变产物称为“子体”,“母体”及其衰变“子体”组成一个衰变链,其称为放射性系列。
4个放射性系列如图1-4。
铀放射性系列可表示为:
238U(不稳定核素)→234Th→234Pa→234U→230Th→226Ra→222Rn→…→206Pb(稳定核素);
钍放射性系列可表示为:
232Th(不稳定核素)→228Ra→228Ac→228Th→224Ra→220Rn→…→208Pb(稳定核素);
锕铀放射性系列可表示为:
235U(不稳定核素)→231Th→231Pa→227Ac→227Th→223Ra→219Rn→…→207Pb(稳定核素)。
除以上3个天然放射系列之外,还有用核反应方法合成的一个人工放射系——镎系:
237Np(不稳定核素)→233Pa→233U→229Th→225Ra→225Ac→221Fr→…→209Bi(稳定核素)。
当然核裂变碎片也往往形成递次衰变的放射系,也属于人工放射系。
依据放射性系列的衰变规律,以及铀—铅同位素演化特征,可以进行放射性定年以及铀地球化学示踪,这对推动铀矿地质理论研究以及指导铀资源勘查具有重要意义。
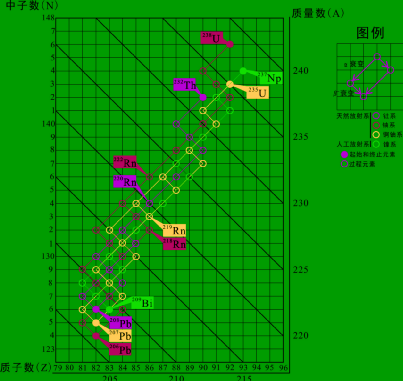
图1-4 4个放射性系列衰变图
打印本页 关闭



